最近の論文発表(原著)
ヒト全遺伝子網羅的探索から明らかになった核酸合成によるオートファジー抑制 (三村, et al., J Biol Chem)
2021年05月12日 最近の論文発表(原著)
Kaito Mimura, Jun-ichi Sakamaki, Hideaki Morishita, Masahito Kawazu, Hiroyuki Mano, Noboru Mizushima
Genome-wide CRISPR screening reveals nucleotide synthesis negatively regulates autophagy
J Biol Chem, S0021-9258(21)00573-1 DOI: https://doi.org/10.1016/j.jbc.2021.100780
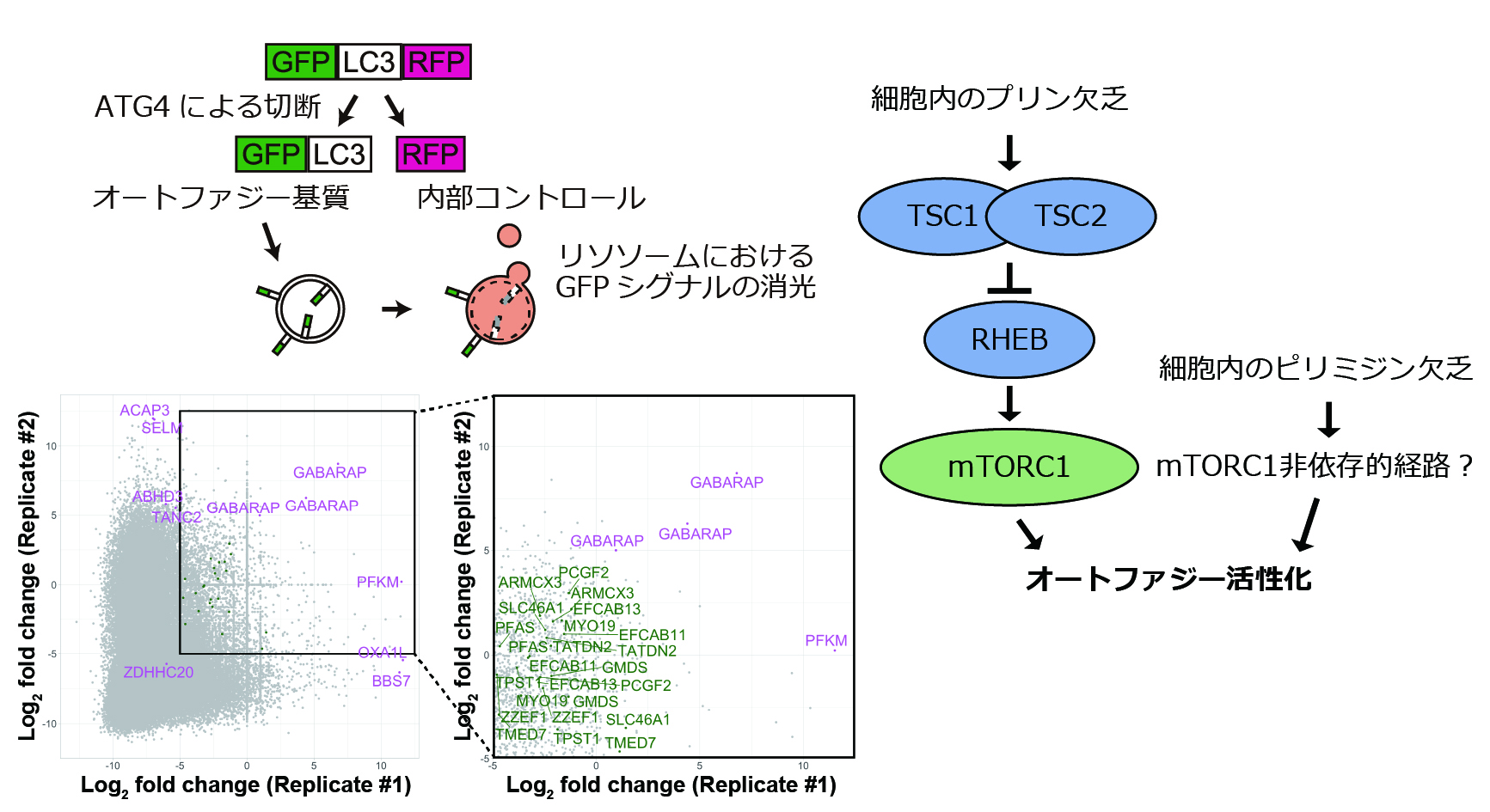
我々はオートファジーの抑制因子を検索するべく、オートファジー活性を定量化できるGFP-LC3-RFPレポーターを使ってゲノムワイドCRISPRスクリーニングを行いました。その結果、プリンのde novo合成経路の1因子であるPFASという酵素の欠損でオートファジーが誘導されることがわかりました。
PFASノックアウト細胞を解析すると、細胞外からのプリン供給が得られない透析血清入りの培地で培養すると強くオートファジーが誘導されることがわかりました。これは細胞内のプリン濃度の低下(プリン飢餓状態)によるものと考えられました。
オートファジーはmTORC1により負に制御されるため、この条件でmTORC1不活化が起きていると予想を立て調べると、確かにプリン飢餓状態ではmTORC1活性が低下していました。さらに、mTORC1の上流因子であるRHEBを抑制するTSC複合体を構成するTSC2のノックアウト細胞を作成すると、この細胞においてはプリン飢餓状態でオートファジーの誘導がほとんど起きませんでした。このことから、プリン飢餓状態におけるオートファジーの活性化はTSC-RHEB-mTORC1のシグナリングに依存していると考えられました。
関連して、ピリミジン合成酵素をノックアウトしたところ、ピリミジン合成経路を構成するCADまたはDHODHのノックアウト細胞においてもオートファジーが活性化するが、mTORC1の活性が低下していないことがわかりました。これにより、プリン欠乏とピリミジン欠乏とでは別個のオートファジー誘導経路が働いていると推測されます。
核酸欠乏は腫瘍の治療で用いられる、メトトレキサートなどの葉酸代謝拮抗薬や5-フルオロウラシルなどの核酸代謝拮抗薬の投与下で起き得ると考えられます。また、腫瘍細胞におけるオートファジーの活性は腫瘍の増殖能に少なからず影響することが報告されており、本研究はオートファジーを用いた腫瘍の治療戦略を考察する上で重要な洞察をもたらすことが期待されます。
本研究は国立がんセンター細胞情報学分野の間野博行博士、河津正人博士と共同で行いました。